Unidad de calor y calor específico
Unidad de Calor
La unidad de calor es la caloría (cal) y la definimos como la cantidad de calor que se necesita 1 gramo de agua para que su temperatura pase de 14,5ºC a 15,5ºC en un lugar donde la presión es de 1 atm.
Parece que esta definición ha caído en desuso como verás más adelante.
Calor específico
Llamamos calor específico a la cantidad de calor, por unidad de masa, necesaria para aumentar 1ºC su temperatura.
Cada sustancia tiene su propio calor específico.
Ejemplos:
SUSTANCIA | CALORÍAS POR GRADO Y GRAMO | ||
Agua | 1,00 | ||
Aceite | 0,45 | ||
Alcohol | 0,67 | ||
Mercurio | 0,03 | ||
Hierro | 0,11 | ||
Aluminio | 0,22 | ||
Cobre | 0,09 | ||
Madera | 0,41 | ||
Mármol | 0,21 | ||
Para resolver problemas que tengan que ver con el cálculo de la Cantidad de calor que necesitamos para que una sustancia alcance una temperatura determinada utilizamos una sencilla fórmula para la que debes tener en cuenta:

La Cantidad de calor (Q) está en razón directa con el calor específico (c), cuanto mayor sea éste mayor será la cantidad de calor que necesita.
La Cantidad de calor (Q) está en razón directa con la masa (m), cuanto mayor sea ésta mayor será la cantidad de calor que necesita.
La Cantidad de calor (Q) está en razón directa con el número de grados a variar (Δt), cuanto mayor sea éste mayor será la cantidad de calor que necesita.
Según las reflexiones anteriores podemos decir que:

4.93 Tenemos 5kg de cobre a una temperatura de 20ºC y necesitamos alcance los 80ºC. Sabiendo que el calor específico del cobre es de 0,09 ¿qué cantidad de calor hemos de proporcionarle?
Respuesta: 27000 cal
Solución
Lo primero que hacemos es pasar los kilos a gramos:
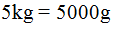
Segundo, calculamos los grados que ha de alcanzar:
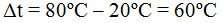
Utilizamos la fórmula, sustituimos valores y obtenemos:
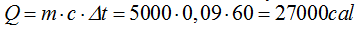
4.94 En la fotografía siguiente vemos una niña calentando un recipiente de acero que contiene 3 litros de agua:

Sabemos que el recipiente pesa 1,8kg y cuando lo coloca al fuego, el recipiente y el agua están a 22ºC.
¿Qué cantidad de calorías se necesitan para que el agua alcance 98ºC sabiendo que el calor específico del acero es, más o menos, de 0,11 cal?
Respuesta: 234048cal
Solución
Como el recipiente y el agua que está en su interior han de alcanzar 98ºC es necesario que calculemos la cantidad de calor que absorbe el recipiente por un lado, y los 3 litros de agua por otro:
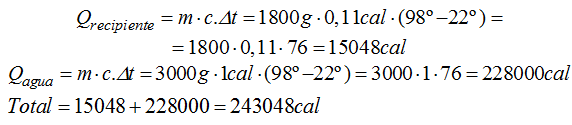
4.95 Un lingote de hierro de 20kg ha absorbido 300000cal.
Sabiendo que el calor específico del hierro es de 0,11cal ¿en cuántos grados hemos incrementado su temperatura?
Respuesta: 136ºC
Solución
No tenemos más que utilizar la fórmula, introducir valores que conocemos y despejar la variable correspondiente:
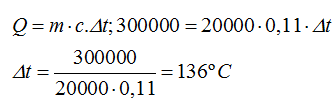
4.96 ¿Cuánto calor cede un recipiente de acero de 500g de peso que contiene 2 litros de agua si ha pasado de 90ºC a 20ºC?
Respuesta: 143850cal
Solución
Aplicamos la fórmula separadamente:
Cantidad de calor que cede el envase:
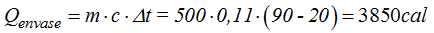
Cantidad de calor que cede el agua:
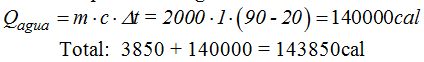
4.97 Se mezclan 10 litros de agua hirviendo con 40 litros de agua a 20ºC. Suponiendo que la temperatura de la mezcla es de 30ºC ¿qué cantidad de calor ha cedido el agua hirviendo?
Respuesta: 700000 cal
Solución
El descenso de la temperatura del agua hirviendo es 100ºC – 30ºC = 70ºC
Cantidad de calor cedido: 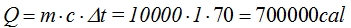
4.98 En un recipiente que contiene 200 litros de agua a 20ºC introducimos un lingote de hierro de 5 kg a una temperatura de 200ºC.
¿Qué temperatura habrá alcanzado el agua una vez realizado el intercambio sucedido entre el calor cedido por el hierro y el ganado por el agua?
Respuesta: 24,82ºC
Solución
Suponiendo T la temperatura alcanzada por el agua y el lingote de hierro tendremos que la temperatura ganada por el agua es de 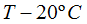 y la cedida por el hierro
y la cedida por el hierro 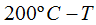 .
.
La cantidad de calor ganada por el agua es:

Como la cantidad de calor ganada es igual a la cedida podemos establecer la siguiente igualdad:
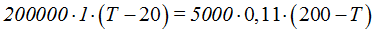
Haciendo operaciones llegamos a:
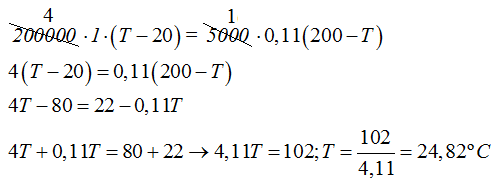
4.99 Tienes un objeto metálico del que no sabes su calor específico. Lo único que sabes de él es lo que pesa, 1kg.
Explica e indica el valor solicitado.
Respuesta: 0,8 cal
Solución
No excluyendo otros modos de resolución, primero calentaría el objeto, por ejemplo, hasta que adquiera 100ºC.
Tomo un recipiente con 2 litros de agua, por ejemplo, que se hallan a 20ºC.
Introduzco el objeto caliente en el recipiente que contiene agua a 20ºC y veo que transcurrido unos segundos, la temperatura del agua ha alcanzado 25ºC.
Llamo k al calor específico del objeto.
Calculo la cantidad de calor cede este objeto al introducirlo en el agua:
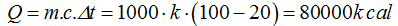
Calculo la cantidad de calor ganada por el agua:
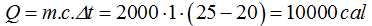
Sin tener en cuenta el recipiente que contiene el objeto y el agua establezco la igualdad de calor cedido = calor ganado:
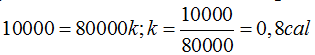
4.100 Emite tu opinión sobre la frase:
“Cuanto mayor es el movimiento de las partículas que forman la materia de un cuerpo, mayor es su temperatura”
Respuesta: Correcta
Si calentamos un cuerpo, las partículas que la componen aumentan su velocidad.

