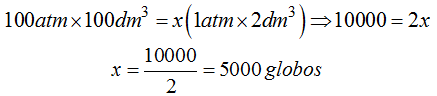Robert Boyle y la relación entre volumen y presión
El señor Boyle, nació en Irlanda el año 1627 en el seno de una familia adinerada, dotado de una gran inteligencia y una gran capacidad de trabajo, desde su infancia se dedicó al estudio e investigación.
En el tema que estamos tratando, relación entre volumen y presión, estableció una ley importante:

A mayor presión, menor volumen, siempre que la temperatura se mantenga invariable.
A menor presión, mayor será el volumen sin variar la temperatura.
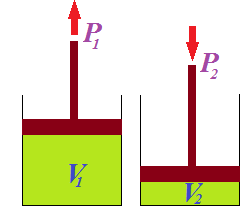
Al observar la figura comprobamos que a medida que aumenta la presión, el volumen disminuye.
Podemos decir, que, el producto de la presión por el volumen para un mismo gas y misma temperatura, el producto de la presión por el volumen se mantiene constante:

Siendo k una constante y teniendo en cuenta la última figura:
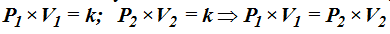
4.76 Un gas en un recipiente cerrado de 280 cm3 se encuentra a una presión de 760mm de mercurio.
Calcula el volumen que ocuparía si la presión aumentase al peso de una barra de mercurio de 860mm de mercurio.
Respuesta: 247,44cm3
Solución
Tomando la fórmula anterior: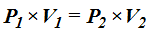
Sustituimos valores: 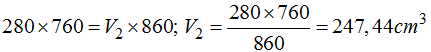
4.77 Imagina que tienes un recipiente con 100 dm3 de gas helio a una presión de 100 atmósferas.
Como son las fiestas del pueblo quieres colaborar soltando unos cuantos globos.
¿Cuántos globos puedes llenar si cada uno es de 2 dm3 y consideras que con una presión de 1 atm puede ascender bien?
Respuesta: 5000 globos
Solución
Supongamos que el número de globos es x y cada uno está representado en cuanto a presión y volumen por P2 y V2
Haciendo uso de 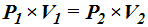 podemos escribir:
podemos escribir: