Formulación química orgánica: compuestos halogenados y oxigenados
1. Formulación química orgánica: compuestos
La formulación y nomenclatura de compuestos orgánicos se caracteriza en que además de cloro e hidrógeno, el compuesto contiene algún átomo más de otro elemento.
Los átomos más habituales, sus valencias y los compuestos orgánicos a los que dan lugar son:
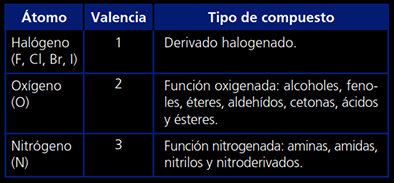
2. Derivados halogenados
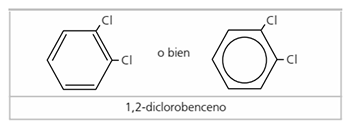
Se nombran anteponiendo el nombre del halógeno (flúor, cloro, bromo o yodo) al nombre del hidrocarburo que lo soporta.
La posición del halógeno se indica mediante el localizador correspondiente.
3. Funciones oxigenadas
3.1 Alcoholes
El grupo funcional es el hidroxilo (OH).
Para nombrar los alcoholes se considera que se ha sustituido un átomo de hidrógeno de un hidrocarburo por el radical OH.
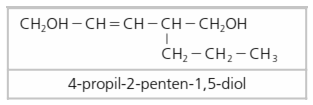
El alcohol obtenido se nombra añadiendo la terminación -ol al hidrocarburo del que procede. Si hay dos grupos alcohol, será -diol, o -triol si son tres.
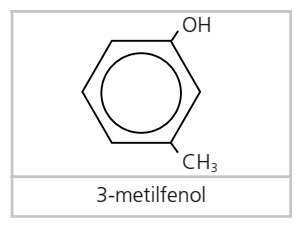
3.2 Fenoles
Son alcoholes derivados del benceno, es decir, obtenidos al sustituir uno o más hidrógenos del benceno por grupos OH.
El más sencillo de la serie es el fenol, que sería el benceno con un grupo OH.
3.3 Éteres
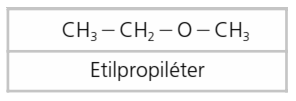
Los éteres están formados por un átomo de oxígeno unido a dos radicales orgánicos.
Se nombran los dos radicales (por tanto, terminados en -il) en orden alfabético y se termina con la palabra éter.
3.4 Aldehídos
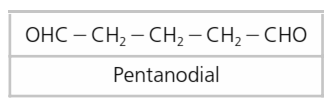
Se caracterizan por tener el grupo CO (grupo carbonilo) siempre en el extremo de la cadena.
Se nombran añadiendo al nombre del hidrocarburo del que derivan el sufijo -al.
Si hay dos grupos aldehído, uno en cada extremo, la terminación será -dial.
3.5 Cetonas
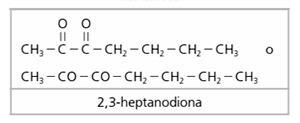
Se caracterizan por tener el grupo CO (grupo carbonilo) en medio de la cadena y no en sus extremos.
Se nombran añadiendo al nombre del hidrocarburo del que derivan el sufijo -ona.
Si hay dos grupos cetona, la terminación será -diona, o -triona si son tres.
3.6 Ácidos carboxílicos
Se caracterizan por tener el grupo carboxilo (COOH) o función ácido en los extremos de la cadena.
Se nombran con el nombre genérico ácido, seguido del nombre del hidrocarburo del que proceden (hidrocarburo con el mismo número de átomos de carbono) terminado en -oico.
Si tiene dos grupos carboxilo, la terminación será -dioico.
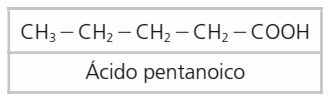
Hay algunos ácidos que mantienen su nombre no sistemático o vulgar, algunos ejemplos son los siguientes:

3.7 Ésteres de los ácidos carboxílicos
Los ésteres se forman mediante la reacción de esterificación entre un ácido y un alcohol.
Los productos de esta reacción son el éster más agua.
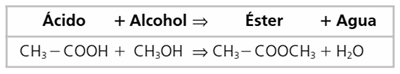
Se nombran cambiando la terminación -ico del ácido por la terminación -ato y, a continuación, el nombre del alcohol en el que cambiamos la terminación -ol por -ilo.
En el ejemplo que hemos puesto, el éster formado se llamará etanoato (acetato) de metilo (el ácido era el etanoico o acético y el alcohol era el metanol).