Formulación química inorgánica: combinaciones binarias del oxígeno
1. Combinaciones binarias del oxígeno
Son combinaciones de oxígeno con otro elemento.
1.1 Según la nomenclatura tradicional
Óxidos: combinaciones de Oxígeno y un metal o de óxigeno y un no metal.
Para formularlos pondremos los símbolos de los elementos que se combinan e intercambiaremos sus valencias, simplificando siempre que sea posible.
Escribiremos siempre en primer lugar el elemento distinto al oxígeno.
Por ejemplo:
(Li → valencia 1) + (O → valencia 2) = Li2O → Óxido de Litio
(Ca → valencia 2) + (O → valencia 2) = Ca2O2→CaO→ Óxido de calcio
Se nombrarán escribiendo la palabra óxido seguido del nombre del metal.
Veamos las distintas opciones según las valencias:
a) Si el elemento que se combina con el oxígeno presenta dos valencias habrá que diferenciar las dos posibilidades.
Por ejemplo:
Fe→ valencia 2 y 3
O → valencia 2
Fe con valencia 3 → Fe2O3 → Óxido Férrico
Fe con valencia 2 → Fe2O2 → FeO → Óxido Ferroso
Escribiremos la palabra óxido seguido del nombre del metal acabado en -ico si actúa con su mayor valencia o acabado en
–oso si actúa con la menor de sus valencias.
b) Si el elemento presenta tres valencias, procederemos de la siguiente manera:
Por ejemplo:
S→ valencia 2, 4 y 6
O→ valencia 2
S con valencia 6 → S2O6 → SO3 → óxido Sulfúrico
S con valencia 4 → S2O4 → SO2 → óxido Sulfuroso
S con valencia 2 → S2O2 → SO → óxido Hiposulfuroso
Es decir, escribiremos la palabra óxido seguido del nombre del no metal acabado en -ico si actúa con su mayor valencia, en -oso si actúa con la valencia intermedia e hipo –oso si aparece la menor de todas.
c) Si el elemento presenta cuatro valencias actuaremos siguiendo este ejemplo:
Por ejemplo:
Cl→ valencias 1,3,5 y 7
O→ valencia 2
Cl con valencia 7 → Cl2O7 → Óxido perclórico
Cl con valencia 5 → Cl2O5 → xido clórico
Cl con valencia 3 → Cl2O3 → óxido cloroso
Cl con valencia 1 → Cl2O → óxido hipocloroso
Así, escribiremos la palabra óxido seguido del nombre del no metal acabado en per -ico si actúa con su mayor valencia, -ico si actúa con la siguiente valencia, en –oso si actúa con la siguiente e hipo –oso si aparece con la menor de todas.
1.2 Nomenclatura de stock
La nomenclatura de stock nombra añadiendo a la palabra óxido el nombre del otro elemento:
Na2O → Óxido de sodio
Si el elemento tiene más de una valencia, ésta se indica en número romano entre paréntesis. Si esta es única no se indica.
Fe2O3 → Óxido de hierro (III)
FeO → Óxido de hierro (II)
SO3 → Óxido de azufre (VI)
(Observa que las fórmulas están simplificadas)
1.3 Nomenclatura sistemática
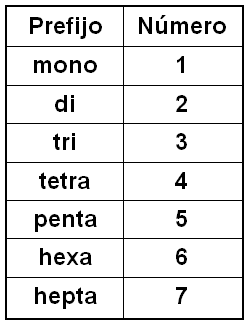
En la nomenclatura sistemática utiliza prefijos para describir la fórmula del compuesto:
Fe2O3 → Trióxido de dihierro